Die Parkinson-Krankheit ist eine fortschreitende neurodegenerative Erkrankung, doch wie sie sich im Gehirn ausbreitet, ist nach wie vor kaum verstanden. Forschern des Luxembourg Center for Systems Biomedicine (LCSB) und internationalen Mitarbeitern ist es nun gelungen, die fortschreitende Ausbreitung der Alpha-Synuclein-Aggregation in einem Assembloid-Modell von Patienten nachzuweisen. Das Verständnis, wie sich toxische Proteinaggregate zwischen Gehirnregionen ausbreiten, ist entscheidend, um die Mechanismen des frühen Krankheitsverlaufs zu entschlüsseln. Die in Advanced Science veröffentlichte Studie liefert neue Erkenntnisse zu diesem Prozess.
Untersuchung der Ausbreitung von Protein-Aggregaten
Während die Parkinson-Krankheit häufig mit Symptomen wie Zittern, Steifheit und verlangsamten Bewegungen in Verbindung gebracht wird, beginnt die Erkrankung in Wirklichkeit bereits im Stillen, lange bevor diese motorischen Symptome auftreten. Das Vorhandensein früher, nicht-motorischer Symptome hat Forscher dazu veranlasst, zu untersuchen, wie sich die Parkinson-Krankheit im Laufe der Zeit im Nervensystem ausbreitet. Eine führende Theorie, die zuerst von dem deutschen Anatomen Prof. Heiko Braak vorgeschlagen wurde, besagt, dass die Parkinson-Krankheit im Darm oder im unteren Hirnstamm beginnt und sich dann allmählich nach einem bestimmten Muster im Gehirn nach oben ausbreitet. Die genauen Mechanismen, die zu dieser Ausbreitung führen, sind jedoch noch unklar.
Im Zentrum der Krankheit steht ein Protein namens Alpha-Synuclein. Im gesunden Gehirn reguliert es die Kommunikation zwischen den Nervenzellen. Bei der Parkinson-Krankheit faltet sich dieses Protein falsch und verklumpt, wodurch Nervenzellen geschädigt werden und abnorme Strukturen entstehen, die als Lewy-Körperchen bekannt sind – ein Schlüsselmerkmal der Krankheit. Um neue Behandlungsstrategien zu entwickeln, ist es wichtig zu verstehen, wie sich diese Aggregate zwischen den Hirnregionen ausbreiten. Um diese Herausforderung zu meistern, hat die Developmental & Cellular Biology Gruppe am LCSB unter der Leitung von Prof. Schwamborn mit Forschern der Technischen Universität Eindhoven, des Universitätsklinikums Schleswig-Holstein in Lübeck und des Hellenic Pasteur Institute in Athen zusammengearbeitet, um die frühen Stadien der Parkinson-Krankheit im Labor mit einem innovativen Werkzeug nachzustellen: Gehirn-Assembloide.
Gehirn-Assembloide: ein neues Modell für die Krankheitsforschung
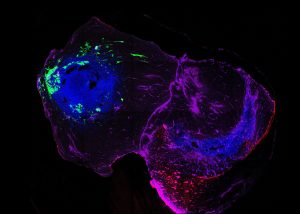
Um das Fortschreiten der Parkinson-Krankheit zu untersuchen, haben die Forscher Assembloide entwickelt, die aus zwei Arten von Gehirn-Organoiden zusammengesetzt sind. Dabei handelt es sich um miniaturisierte Hirnstrukturen, die aus menschlichen Stammzellen im Labor gezüchtet wurden. Ein Organoid stellte das Hinterhirn dar, wo die Parkinson-Krankheit vermutlich beginnt, das andere das Mittelhirn, in dem sich die Dopamin produzierenden Nervenzellen befinden, die bei der Krankheit zerstört werden.
Unter Verwendung von induzierten pluripotenten Stammzellen (iPSCs), die von Parkinson-Patienten mit einer seltenen SNCA-Gentriplikation stammen, einer Mutation, die zu einer Überproduktion von Alpha-Synuclein führt, stellte das Team fest, dass die Hinterhirn-Organoide spontan toxische Proteinaggregate bildeten. Als diese dann mit gesunden Mittelhirn-Organoiden zu einem Assembloid verbunden wurden, begann sich die Alpha-Synuclein-Pathologie innerhalb von nur 30 Tagen auf das gesunde Mittelhirngewebe auszubreiten.
„Dieses vom Patienten stammende Assembloid-Modell gibt uns einen beispiellosen Einblick in die Art und Weise, wie sich das toxische Alpha-Synuclein ansammelt und zwischen den Hirnregionen ausbreitet“, erklärt Prof. Jens Schwamborn. „Es ist das erste Mal, dass wir das Fortschreiten dieser Pathologie in einem auf dem Menschen basierenden System beobachten konnten, ohne das Protein übermäßig zu exprimieren oder auf künstliche Auslöser angewiesen zu sein“. Die Studie liefert somit einen direkten Beweis für Braaks Hypothese und zeigt, dass sich toxische Alpha-Synuclein-Aggregate von einer Hirnregion zur anderen ausbreiten können.
Alpha-Synuclein und seine Rolle beim Fortschreiten der Parkinson-Krankheit
Die Studie zeigte, dass ein Überschuss an Alpha-Synuclein im Hinterhirn ausreicht, um seine Ausbreitung ins Mittelhirn auszulösen und die Synapsen – die lebenswichtigen Kommunikationspunkte zwischen den Nervenzellen – zu schädigen.Noch bevor die Nervenzellen abzusterben begannen, beobachteten die Forscher frühe Anzeichen einer synaptischen Dysfunktion, einem Schlüsselmerkmal der Neurodegeneration.
„Ein Anstieg von Alpha-Synuclein im Hinterhirn reichte aus, um die Ausbreitung des pathologischen Alpha-Synuclein-Proteins in das gesunde Mittelhirn auszulösen, was zu einer synaptischen Dysfunktion führte“, erklärt Prof. Schwamborn. „Dies macht das Modell geeignet für zukünftige Anwendungen, um sowohl den Prozess der Ausbreitung der Pathologie besser zu verstehen als auch therapeutische Ansätze zu entwickeln, die diesen Prozess hemmen.“
Das Team nutzte auch fortgeschrittene Techniken wie Mikroelektroden-Arrays und Virus-Tracking, um zu bestätigen, dass die Organoide funktionelle, gerichtete Verbindungen bilden, genau wie echte Hirnregionen. Als sich Alpha-Synuclein ausbreitete, wurden diese Verbindungen schwächer, was auf eine frühe Unterbrechung der Netzwerkaktivität im Gehirn hindeutet.
Auf dem Weg zu Früherkennung und personalisierter Medizin.
Assembloide bieten eine kontrollierte Umgebung, in der das Fortschreiten der Parkinson-Krankheit mit bisher unerreichter Detailgenauigkeit untersucht werden kann. Da sie die natürliche Architektur und Konnektivität des Gehirns nachahmen, versprechen sie nicht nur, die frühesten Ereignisse der Parkinson-Krankheit aufzudecken, sondern auch neue Ansätze für die Präzisionsmedizin. Da die Organoide von einzelnen Patienten stammen, können die Forscher untersuchen, wie sich bestimmte genetische Hintergründe auf den Krankheitsverlauf auswirken, und gezielte Therapien testen.
„Dieses Modell bietet eine einzigartige Möglichkeit, frühe Krankheitsmechanismen zu untersuchen und nach Medikamenten zu suchen, die die Vermehrung von Alpha-Synuclein blockieren können, bevor irreversible Schäden auftreten“, sagt Prof. Schwamborn. „Letztendlich könnte dies zu präventiven Therapien für Menschen mit hohem genetischen Risiko führen, die die Krankheit stoppen, bevor sie sich ausbreitet.
—
Wissenschaftiche Publikation: Gomez-Giro G, Frangenberg D, Vega D, Zagare A, Barmpa K, Antony PMA, Robertson G, Sabahi-Kaviani R, Haendler K, Kruse N, Papastefanaki F, Matsas R, Spielman M, Luttge R and Schwamborn JC. Alpha-synuclein pathology spreads in a midbrain-hindbrain assembloid model. Advanced Science, April 2025.
Finanzierung: Diese Forschung wurde durch das Forschungs- und Innovationsprogramm Horizont 2020 der Europäischen Union unterstützt.
Titelbild: Gemma Gomez-Giro.